




INVESTICE DO ROZVOJE VZDĚLÁVÁNÍ
Výukové materiály ZŠ Kaplice, Školní 226





- Úvod
- Přehled hlavních derivátů uhlovodíků
- Halogenové deriváty
- Alkoholy a fenoly
- Karbonylové sloučeniny
- Karboxylové kyseliny
- Estery
Úvod
Uhlovodíky patří k základním organickým sloučeninám.
I když tvoří malou část organických sloučenin, můžeme od nich odvozovat další tisíce organických látek - podle latinského slova "derivate" = odvozovat, nazývají se tyto sloučeniny deriváty.
Definice derivátů uhlovodíků
Deriváty uhlovodíků jsou organické sloučeniny, jejichž molekuly obsahují vedle uhlíku a vodíku i jiné prvky (např. kyslík, dusík, halogeny, síru atd.) Jejich vzorce se odvozují náhradou atomů vodíku v molekule uhlovodíku atomy nebo skupinami atomů jiných prvků tzv. charakteristickou skupinou (-Cl, -OH, -CO).
Příklady
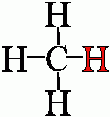
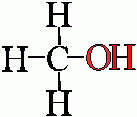
Uhlovodíkový zbytek (např. alkanů - alkyl, arenů - aryl) - je část molekuly bez jednoho či více atomů vodíku, v názvu koncovka -yl, zkratka zbytku R
Uhlovodík (U) - vodík ---> Uhlovodíkový zbytek (R)

- H --->
Uhlovodíkový zbytek arenů je aren bez jednoho nebo více atomů vodíku.
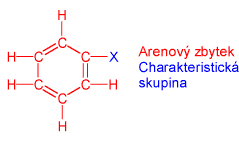
Příklady uhlovodíkových zbytků:
Uhlovodík Uhlovodíkový zbytek vzorec název vzorec název CH4 methan CH3- methyl C2H6 ethan C2H5- ethyl C3H8 propan C3H7- propyl C4H10 butan C4H9- butyl
nahoru
Přehled hlavních derivátů uhlovodíků
DERIVÁTY UHLOVODÍKŮ Název derivátů Charakteristická skupina Obecný vzorec Příklad vzorec název Halogenové deriváty uhlovodíků X: -F, -Cl, -Br, -I R-X
R: alkyl, arylCH3Cl chlormethan Kyslíkaté deriváty
uhlovodíkůAlkoholy -OH R-OH
R: alkylC2H5OH ethanol Fenoly -OH R-OH
R: arylC6H5OH fenol Aldehydy -CH=O RCHO CH3CHO ethanal Ketony -C=O RCOR´ CH3COCH3 propanon Karboxylové kyseliny -COOH R-COOH CH3COOH kyselina ethanová Aminokyseliny -COOH, -NH2 CH3CH(NH2)COOH kyselina aminopropanová Estery -O-C=O R-COOR´ CH3COOCH3 methylester
kyseliny ethanové
Uhlovodíkové zbytky R, R´ u ketonů a esterů mohou být u dané látky stejné (viz příklad v této tabulce) nebo rozdílné.
nahoru
Halogenové deriváty
Definice
Jsou to deriváty uhlovodíků, ve kterých charakteristickou skupinou tvoří atomy halogenů (F, Cl, Br, I).
Obecný vzorec
R - X
R - uhlovodíkový zbytek
X - halogen (F, Cl, Br, I)
Názvosloví
Názvy halogenových derivátů se přednostně tvoří pomocí předpon fluor-, chlor-, brom- nebo jod-, které určují název charakteristické skupiny a z uhlovodíkového zbytku .
Příklad 1:
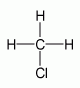
1. Určíme charakteristickou skupinu - chlor, takže první část názvu této sloučeniny bude předpona chlor-.
2. Určíme uhlovodíkový zbytek CH3- je od methanu, to znamená, že druhou část názvu bude tvořit slovo -methan.
3. Spojíme-li obě části, dostaneme celý název sloučeniny chlormethan.
Příklad 2:
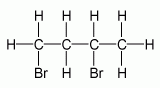
1. Určíme charakteristickou skupinu - brom. Název této sloučeniny bude tvořit předpona brom-, ale ještě před ní bude číslovková předpona di-, protože bromy jsou dva.
2. Určíme uhlovodíkový zbytek - je od butanu, to znamená, že třetí část názvu bude tvořit slovo -butan.
3. Spojením všech tří částí dostaneme název - dibrombutan. Na závěr ještě určíme přesnější polohu bromů - jsou na prvním a třetím uhlíku. Tuto skutečnost zapíšeme před už námi zjištěný název následujícím způsobem: 1, 3 - dibrombutan.
Příklady
Název Strukturní vzorec Racionální vzorec Molekulový vzorec Použití (význam) tetrachlormethan CCl4 CCl4 kapalná látka, karcinogenní vlastnosti,
jedovatá se používá jako rozpouštědlotetrafluorethylen CF2=CF2 C2F4 surovina pro výrobu plastů,
výroba teflonuvinylchlorid CH2=CHCl C2H3Cl výroba polyvinylchloridu (PVC) freon
dichlor-difluormethanCCl2F2 Freony poškozují atmosféru.
nahoru
Alkoholy
Definice
Alkoholy jsou deriváty uhlovodíků, které mají v molekule hydroxylovou skupinu -OH vázanou na nearomatický uhlovodíkový zbytek.
Obecný vzorec
R - OH
R - nearomatický uhlovodíkový zbytek
OH - hydroxylová skupina
Názvosloví
Názvy alkoholů se tvoří pomocí koncovky -ol připojené k názvu příslušného uhlovodíku.
Příklad :
1. Zjistíme název uhlovodíku, od kterého byl tento alkohol odvozen. Je to propan.
2. Připojíme k zjištěnému uhlovodíku koncovku -ol.
3. Propan + -ol = propanol
Příklady alkoholů
Název Strukturní vzorec Racionální vzorec Molekulový vzorec methanol CH3OH CH3OH ethanol CH3CH2OH C2H5OH ethylenglykol
(ethan-1,2-diol)HOCH2CH2OH C2H4(OH)2 glycerol
(propan-1,2,3-triol)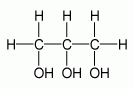
HOCH2CHOHCH2OH C3H5(OH)3
Zástupci alkoholů
Název Vlastnosti Využití methanol bezbarvá, kapalná, hořlavá, prudce jedovatá látka rozpouštědlo, výroba formaldehydu, kapalné palivo ethanol specificky vonící, bezbarvá, hořlavá kapalina výroba chemikálií a alkoholických nápojů, používá se jako rozpouštědlo, jako palivo nebo dezinfekční prostředek ethylenglykol velmi jedovatá, bezbarvá, olejovitá kapalina neomezeně mísitelná s vodou složka do nemrznoucích chladicích přístrojů, surovina pro výrobu plastů glycerol bezbarvá, olejovitá kapalina s nasládlou chutí používá se k výrobě výbušnín, v kosmetice a v potravinářství
Fenoly
Definice
Fenoly jsou sloučeniny, ve kterých je hydroxylová skupina vázána na uhlovodíkový zbytek arenů.
Obecný vzorec
Ar -OH
Ar - arenový zbytek
OH - hydroxylová skupina
Příklady
Název Strukturní vzorec Racionální vzorec Molekulový vzorec fenol
C6H5OHC6H6O kresol 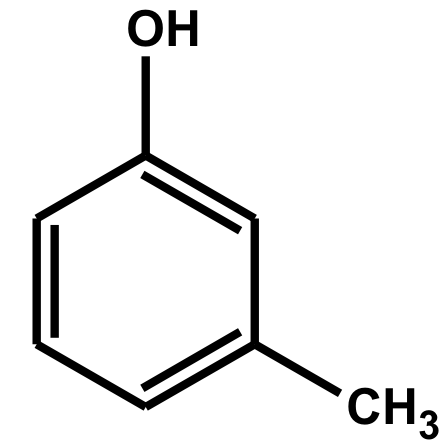
C6H4CH3OH C7H8O
obr. wikipedie.cz
Zástupci
Fenol C6H5OH
obr. wikipedie.cz
- jedovatá, bezbarvá, krystalická látka
- používá se při výrobě barviv, plastů, léčiv
nahoru
Karbonylové sloučeniny
Karbonylové sloučeniny jsou deriváty uhlovodíků, které obsahují karbonylovou skupinu:
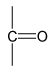
Tyto sloučeniny dělíme na aldehydy a ketony.
Aldehydy
Definice
Aldehydy jsou deriváty uhlovodíků, ve kterých je ke karbonylové skupině vázán atom vodíku a uhlovodíkový zbytek.
Obecný vzorec
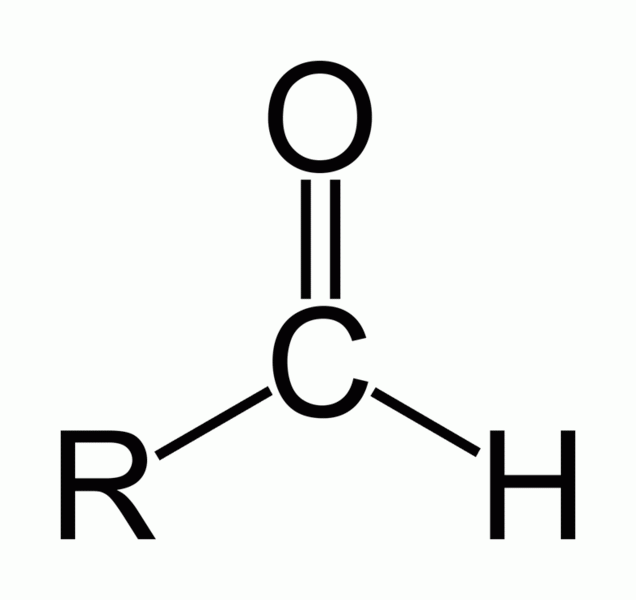
Názvosloví
Názvy aldehydů se tvoří pomocí přípony -al, která se přidá k názvu základního uhlovodíku. Při určování počtu uhlíkových atomů je třeba počítat i uhlíkový atom karbonylové skupiny.
Příklad
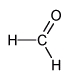
1. Název základního uhlovodíku je methan.
2. K tomuto názvu připojíme příponu -al.
3. methan + -al = methanal
Příklady aldehydů
Název Strukturní vzorec Racionální vzorec Molekulový vzorec methanal
(formaldehyd)HCHO CH2O ethanal
(acetaldehyd)CH3-CHO C2H4O
Zástupci
Methanal (formaldehyd)
- bezbarvá, plynná a jedovatá látka
- dezinfekční a konzervační prostředek, surovina pro výrobu plastů
Ethanal (acetaldehyd)
- kapalná látka
- výroba kaučuku, léčiv a barviv
Ketony
Definice
Ketony jsou deriváty uhlovodíků, ve kterých jsou ke karbonylové skupině vázány dva uhlovodíkové zbytky.
Obecný vzorec
Názvosloví
Systematické názvy ketonů se tvoří dvěma způsoby (existují také názvy triviální).
Příklad
a) První způsob:
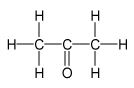
1. Název základního uhlovodíku je propan.
2. K tomuto názvu připojíme příponu -on.
3. propan + -on = propanon
b) Druhý způsob:
CH3 je uhlovodíkový zbytek methanu, který se nazývá methyl. Methyly jsou zde dva, takže je to dimethyl + keton = dimethylketon (triviální název - aceton)
Zástupci
Aceton
(propanon)CH3COCH3 C3H6O
- bezbarvá hořlavá kapalina charakteristicky zapáchající
- používá se jako rozpouštědlo barev a laků, k výrobě léčiv (chloroform, jodoform, sulfonal aj.) a plastů (plexisklo)
nahoru
Karboxylové kyseliny
Definice
Karboxylové kyseliny jsou deriváty uhlovodíků, které obsahují karboxylovou skupinu:

Obecný vzorec:
Názvosloví
Názvy monokarboxylových kyselin se odvozují od uhlovodíků.
- název uhlovodíku + přípona-ová kyselina
Př. CH3(CH2)2COOH
butanová kyselina (odvozena od butanu)
- často používáme triviální názvy, zde např. kyselina máselná CH3(CH2)2COOH
Příklady
Název Strukturní vzorec Racionální vzorec Vlastnosti Využití kyselina methanová
(kyselina mravenčí)HCOOH kapalina, součást mravenčího jedu jako konzervační a dezinfekční prostředek kyselina ethanová
(kyselina octová)CH3COOH štiplavě páchnoucí kapalina, leptá pokožku výroba barviv, plastů, konzervace potravin
Chemické vlastnosti karboxylových kyselin
K nejvýznamnějším reakcím karboxylových kyselin patří ty, které obdobně probíhají i u kyselin anorganických.
1) ionizace: CH3COOH ---> CH3COO- + H+
2) reakce s hydroxidy (reakce neutralizační); vzniká sůl karboxylové kyseliny a voda:
CH3COOH + KOH ---> CH3COOK + H2O
kyselina octová + hydroxid draselný ---> octan draselný + voda
3) reakcí s kovy vzniká sůl karboxylové kyseliny a vodík
2CH3COOH + 2Na ---> 2CH3COONa + H2
kyselina octová + sodík ---> octan sodný + vodík
4) reakce s alkoholy (reakce esterifikační); vzniká ester karboxylové kyseliny a voda:
CH3COOH + CH3OH ---> CH3COOCH3 + H2O
kyselina octová + methanol ---> methylester kyseliny octové + voda
Karboxylové kyseliny v domácnosti:
1. Kyselina citronová je slabá karboxylová kyselina nacházející se v citrusových plodech. Používá se jako konzervační látka a jako dochucovací prostředek jídel a nealkoholických nápojů (bývá označována pod E330).
obr. www. wikipedie.cz, www.oetker.cz
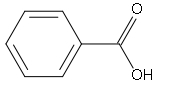
2. Kyselina benzoová je nejjednodušší aromatická jednosytná karboxylová kyselina. Využívá se jako konzervační prostředek (E210) a léčivo proti kožním infekcím.
3. Karboxylové kyseliny vázané v tucích:
racionální vzorec zkracený
racionální
vzorecnázev (triviální) použití CH3-(CH2)14-COOH C15H31COOH kyselina palmitová výroba mýdel a kosmetiky CH3-(CH2)16-COOH C17H35COOH kyselina stearová výroba mýdel a kosmetiky CH3-(CH2)7-CH=CH-(CH2)7-COOH C17H33COOH kyselina olejová potravina (vitamin F)
Aminokyseliny
Jsou to karboxylové kyseliny, které jsou obsaženy ve všech živých organizmech a mají charakteristickou aminovou skupinu -NH2.
Aminokyseliny jsou stavební jednotky peptidů a bílkovin, v jejichž molekulách jsou vázány peptidovou vazbou -CO-NH-.
Na stavbě molekul peptidů a bílkovin se podílí celkem dvacet aminokyselin.
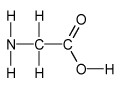
Příklad: kyselina aminooctová (glycin)
nahoru
Estery
Definice
Jsou to produkty reakce karboxylových kyselin a alkoholů.
karboxylová kyselina + alkohol ---> ester + voda
Příklad
CH3 -COOH + HO-CH2-CH3 ---> CH3-CO-O-CH2-CH3 + H2O
kyselina octová + ethanol ---> ethylester kyseliny octové + voda
Chemická reakce kyseliny s alkoholem, při které vzniká ester a voda se nazývá esterifikace.
Příklad
ethylester kyseliny octové
CH3COOCH2CH3
K esterům patří chemické výrobky i přírodní látky.
Estery se používají jako rozpouštědla, paliva či léčiva.
Kapalné estery většinou příjemně voní a vyskytují se hlavně v ovoci.
Charakter vůně některých esterů vzniklých reakcí karboxylových kyselin a alkoholů:
ester vůně ethylester kyseliny mravenčí rumová penthylester kyseliny octové banánová oktylester kyseliny octové pomerančová ethylester kyseliny máselné ananasová ethylester kyseliny benzoové mátová penthylester kyseliny máselné meruňková